
第 1 页 / 共 19 页
答案陈钟秀_第1页_学霸英雄_www.xuebayingxiong.com.png)
第 2 页 / 共 19 页
答案陈钟秀_第2页_学霸英雄_www.xuebayingxiong.com.png)
第 3 页 / 共 19 页
课后答案完整版-朱自强_第1页_学霸英雄_www.xuebayingxiong.com.png)
第 4 页 / 共 19 页
课后答案完整版-朱自强_第2页_学霸英雄_www.xuebayingxiong.com.png)
第 5 页 / 共 19 页

第 6 页 / 共 19 页

第 7 页 / 共 19 页

第 8 页 / 共 19 页

第 9 页 / 共 19 页

第 10 页 / 共 19 页

第 11 页 / 共 19 页

第 12 页 / 共 19 页

第 13 页 / 共 19 页

第 14 页 / 共 19 页

第 15 页 / 共 19 页

第 16 页 / 共 19 页

第 17 页 / 共 19 页
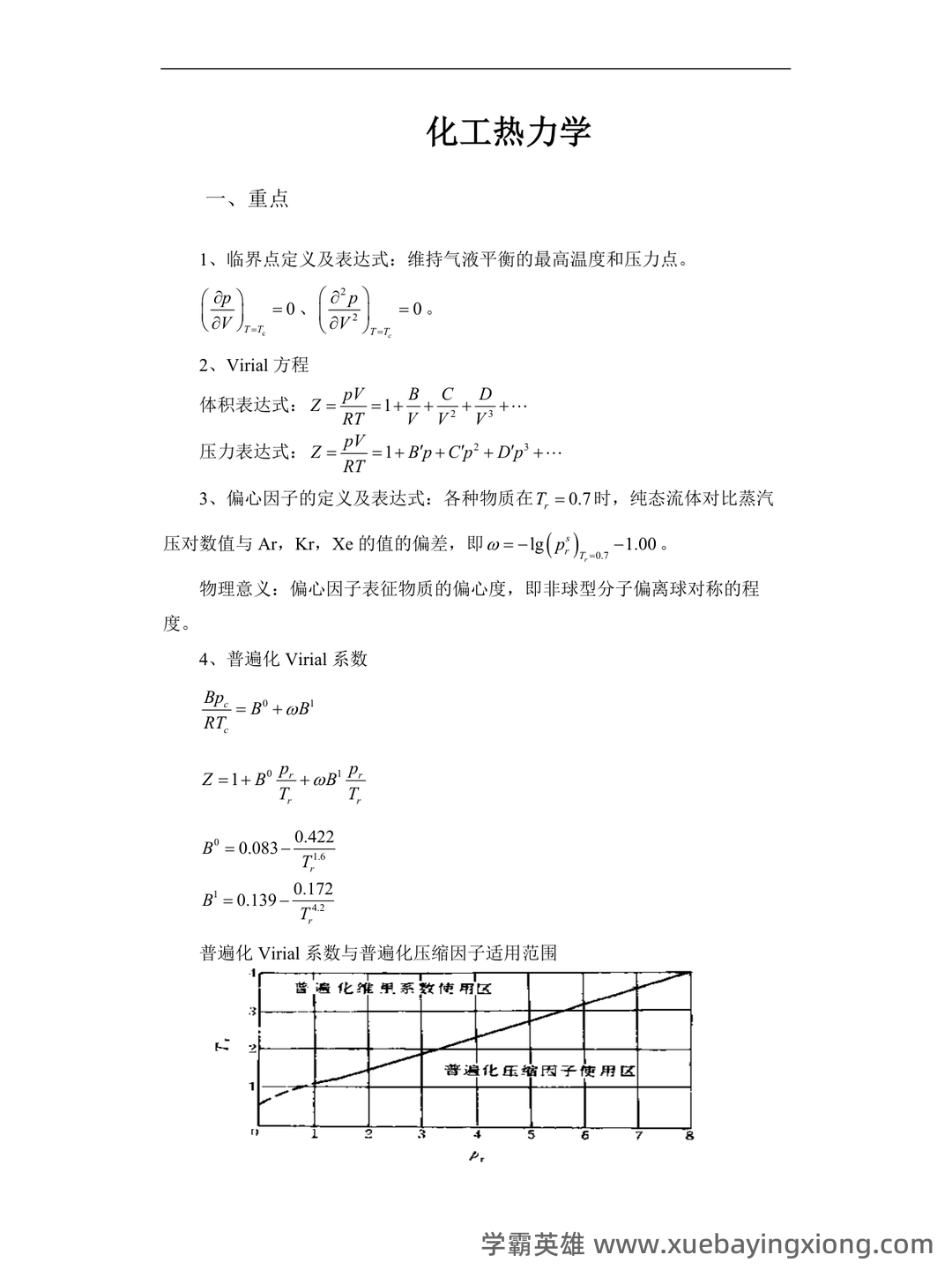
第 18 页 / 共 19 页

第 19 页 / 共 19 页
化工热力学名词解释
化工热力学名词解释 在复杂的化工生产过程中,我们常常会遇到各种各样的热力学名词。理解这些术语是保障生产安全、提高效率的关键。今天,我们就来梳理一下化工热力学中一些核心的词汇,希望对大家有所帮助。 首先,我们必须明确什么是化工热力学。它实际上是运用热力学原理来研究化工过程的学科。简单来说,就是利用热力学定律来分析和预测化学反应和物理变化过程中涉及的能量传递和状态变化。这不仅仅是理论知识,更是应用于工业实践的基石。 接下来,我们来看看几个重要的概念。焓(H),是热力学系统总的能量表示,包含内能和压力乘以体积。理解焓的变化,就能判断反应是否自发进行。再比如,熵(S),它代表着系统的无序程度,一个反应熵增意味着系统变得更加无序。 吉布斯自由能(G)则提供了判断反应是否自发进行更全面的信息,它考虑了焓变和熵变。在化工热力学中,吉布斯自由能是判断反应自发性最常用的指标之一。同时,热力学平衡,是指系统达到平衡状态时的稳定状态,此时系统内部的各个物理量不再发生变化。 此外,相变也是化工热力学研究的重要内容。比如液化、汽化、升华等过程,都会伴随热量的吸收或释放,这些变化都受到了热力学原理的严格控制。 最后,要记住 热力学定律,包括能量守恒定律和熵增定律。这些定律是化工热力学的基础,任何计算和分析都必须建立在这条理论基础上。
展开
化工热力学
2025-07-12
13次阅读